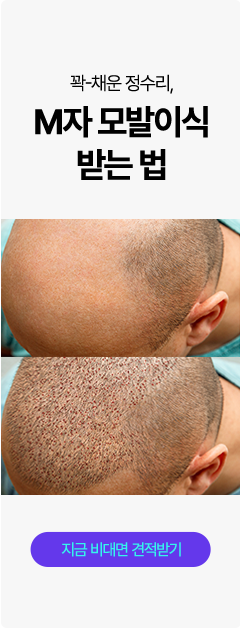
-
모발이식 후 좌우비대칭이셨던분들 있을까요?
K34642691922405030231님
-
밀도가 낮은거 아닌가요?
한발더님
-
-
모발이식 실패인건가요? 2주차 다되어갑니다
젠장망할탈모님
-
모발이식 실패와 부작용
대강철저님
-
모발이식 후 좌우비대칭이셨던분들 있을까요?
K34642691922405030231님
지금, 모발이식 검색해보세요
1.
모발이식
2.
대구
3.
정수리
4.
부산
5.
박상현
6.
모제림
7.
미녹시딜
8.
탈모성지
9.
핀페시아
10.
몰린
지금, 모발이식 검색해보세요
전체 13,008건
전체 8,955건
전체 26,354건








 모션모발이식의원
모션모발이식의원 
 연세미다인
연세미다인 
 모빈치모발이식센터
모빈치모발이식센터 
 JP성형외과
JP성형외과